L'hypoalgésie induite par l'exercice (EIH) décrit une forte réduction de la sensibilité à la douleur après l'exercice. Elle se caractérise par un seuil de douleur élevé ou diminution de l’intensité de la douleur au-dessus du seuil, évalués à l'aide de stimuli nocifs tels que la température, la stimulation électrique et la pression mécanique.
La réduction de la sensibilité à la douleur est plus importante dans le membre qui fait de l'exercice, mais on l’observe également dans des zones éloignées du corps ne faisant pas d'exercice, ce qui suggère que les manifestations locales et les voies nociceptives spinales/supraspinales sont impliquées dans l'inhibition de la douleur avec exercice.
Les modèles de recherche sur l'homme et l'animal ont identifié plusieurs mécanismes possibles susceptibles de déclencher l'EIH.
- La modulation conditionnée de la douleur (CPM)
- Le recrutement d'unités motrices à seuil élevé
- Le lien entre les barorécepteurs et les voies de la douleur
- La douleur induite par l'ischémie et les métabolites, qui sont collectivement considérés comme déclenchant des voies descendantes inhibitrices de la douleur.
L’EIH peut également être provoqué par des substances produites de manière endogène qui ont des effets antinociceptifs. L'une de ces substances est la bêta-endorphine (BE), un neuropeptide opioïde dont on a montré qu'il augmentait en concentration après un exercice physique chez l'homme.
On pense que cette augmentation est due à la stimulation des fibres afférentes des groupes III et IV dans le muscle contracté, activant le système opioïde. Les recherches démontrant l'atténuation de l'EIH, avec l'administration d'un agoniste opioïde tel que la naloxone, soutiennent le rôle du système opioïde dans l'EIH.
Une hypoalgésie insensible aux antagonistes des opioïdes suggère que des mécanismes non opioïdes contribuent à l'EIH. L'un de ces mécanismes est le système endocannabinoïde (ECB). Les endocannabinoïdes sont synthétisés et rapidement libérés des cellules en réponse à des conditions stressantes telles que l'exercice physique.
Des études ont rapporté des concentrations accrues d'endocannabinoïdes après l'exercice chez l'homme, ce qui suggère que le système ECB pourrait contribuer à l'EIH.
L'effet analgésique de l'exercice est devenu important dans les programmes de gestion de la douleur. Les preuves actuelles démontrent l'efficacité de l'exercice de résistance pour réduire la douleur chez les personnes souffrant de douleurs chroniques. L'effet analgésique semble plus important avec une intensité plus élevée et un exercice prolongé. Par exemple, un effet important a été observé avec un exercice de résistance avec une charge externe utilisée supérieure à 75 % du maximum d'une répétition (1RM).
Cependant, les personnes souffrant de douleurs chroniques sont souvent limitées au niveau de la charge, et les charges lourdes peuvent entraîner une hyperalgésie. Lors d'exercices à faible intensité, le fait de prolonger la durée de l'exercice en exécutant la tâche jusqu'à l'échec peut augmenter l'EIH. Cependant, cela peut prendre un temps considérable et peut donc ne pas être pratique chez les personnes souffrant de douleurs chroniques.
Des recherches récentes suggèrent que la pratique d'exercices de résistance à faible charge avec restriction du flux sanguin (BFR-RE) peut avoir un effet de modulation de la douleur. Le BFR-RE implique une restriction partielle et totale du flux sanguin artériel et veineux, dans le membre actif lors de l'exercice avec des charges de 20 à 30 % de 1RM.
Il est largement connu pour augmenter l'hypertrophie musculaire et les adaptations de force par rapport à un exercice d'intensité équivalente sans BFR.
Le BFR-RE produit également un effet sur l’EIH et il a été démontré qu'il réduit la douleur dans le cadre d'un programme d'entraînement chez les personnes souffrant d'une pathologie du genou. Pour les populations ne pouvant pas supporter un exercice à haute intensité ou un exercice à faible intensité jusqu'à l'échec, le BFR-RE aurait donc un double effet sur la douleur et les adaptations musculaires.
Toutefois, l'EIH avec le BFR-RE par rapport à une forme équivalente d'exercice à la fois à faible et à forte intensité n'a pas été examinée, et l'effet sur les systèmes opioïdes et ECB est inconnu.
Par conséquent, le but de cette étude était de comparer l’intensité de l'EIH avec le BFR-RE (pression basse et haute), à l'exercice de résistance (intensité basse et haute).
On a émis l'hypothèse que le BFR-RE augmenterait la réponse EIH par rapport à l’exercice de résistance à faible charge (LLRE), et qui serait augmenté à un niveau similaire l’exercice de résistance à charge lourde (HLRE) par l'utilisation d'une pression plus élevée.
La réduction de la sensibilité à la douleur est plus importante dans le membre qui fait de l'exercice, mais on l’observe également dans des zones éloignées du corps ne faisant pas d'exercice, ce qui suggère que les manifestations locales et les voies nociceptives spinales/supraspinales sont impliquées dans l'inhibition de la douleur avec exercice.
Les modèles de recherche sur l'homme et l'animal ont identifié plusieurs mécanismes possibles susceptibles de déclencher l'EIH.
- La modulation conditionnée de la douleur (CPM)
- Le recrutement d'unités motrices à seuil élevé
- Le lien entre les barorécepteurs et les voies de la douleur
- La douleur induite par l'ischémie et les métabolites, qui sont collectivement considérés comme déclenchant des voies descendantes inhibitrices de la douleur.
L’EIH peut également être provoqué par des substances produites de manière endogène qui ont des effets antinociceptifs. L'une de ces substances est la bêta-endorphine (BE), un neuropeptide opioïde dont on a montré qu'il augmentait en concentration après un exercice physique chez l'homme.
On pense que cette augmentation est due à la stimulation des fibres afférentes des groupes III et IV dans le muscle contracté, activant le système opioïde. Les recherches démontrant l'atténuation de l'EIH, avec l'administration d'un agoniste opioïde tel que la naloxone, soutiennent le rôle du système opioïde dans l'EIH.
Une hypoalgésie insensible aux antagonistes des opioïdes suggère que des mécanismes non opioïdes contribuent à l'EIH. L'un de ces mécanismes est le système endocannabinoïde (ECB). Les endocannabinoïdes sont synthétisés et rapidement libérés des cellules en réponse à des conditions stressantes telles que l'exercice physique.
Des études ont rapporté des concentrations accrues d'endocannabinoïdes après l'exercice chez l'homme, ce qui suggère que le système ECB pourrait contribuer à l'EIH.
L'effet analgésique de l'exercice est devenu important dans les programmes de gestion de la douleur. Les preuves actuelles démontrent l'efficacité de l'exercice de résistance pour réduire la douleur chez les personnes souffrant de douleurs chroniques. L'effet analgésique semble plus important avec une intensité plus élevée et un exercice prolongé. Par exemple, un effet important a été observé avec un exercice de résistance avec une charge externe utilisée supérieure à 75 % du maximum d'une répétition (1RM).
Cependant, les personnes souffrant de douleurs chroniques sont souvent limitées au niveau de la charge, et les charges lourdes peuvent entraîner une hyperalgésie. Lors d'exercices à faible intensité, le fait de prolonger la durée de l'exercice en exécutant la tâche jusqu'à l'échec peut augmenter l'EIH. Cependant, cela peut prendre un temps considérable et peut donc ne pas être pratique chez les personnes souffrant de douleurs chroniques.
Des recherches récentes suggèrent que la pratique d'exercices de résistance à faible charge avec restriction du flux sanguin (BFR-RE) peut avoir un effet de modulation de la douleur. Le BFR-RE implique une restriction partielle et totale du flux sanguin artériel et veineux, dans le membre actif lors de l'exercice avec des charges de 20 à 30 % de 1RM.
Il est largement connu pour augmenter l'hypertrophie musculaire et les adaptations de force par rapport à un exercice d'intensité équivalente sans BFR.
Le BFR-RE produit également un effet sur l’EIH et il a été démontré qu'il réduit la douleur dans le cadre d'un programme d'entraînement chez les personnes souffrant d'une pathologie du genou. Pour les populations ne pouvant pas supporter un exercice à haute intensité ou un exercice à faible intensité jusqu'à l'échec, le BFR-RE aurait donc un double effet sur la douleur et les adaptations musculaires.
Toutefois, l'EIH avec le BFR-RE par rapport à une forme équivalente d'exercice à la fois à faible et à forte intensité n'a pas été examinée, et l'effet sur les systèmes opioïdes et ECB est inconnu.
Par conséquent, le but de cette étude était de comparer l’intensité de l'EIH avec le BFR-RE (pression basse et haute), à l'exercice de résistance (intensité basse et haute).
On a émis l'hypothèse que le BFR-RE augmenterait la réponse EIH par rapport à l’exercice de résistance à faible charge (LLRE), et qui serait augmenté à un niveau similaire l’exercice de résistance à charge lourde (HLRE) par l'utilisation d'une pression plus élevée.
Matériels et méthodes
Douze personnes ont réalisé quatre essais expérimentaux impliquant un exercice unilatéral (leg press) :
Quatre protocoles d'exercices de résistance ont été utilisés dans un ordre aléatoire, dont
1) Exercice de résistance à charge légère (LLRE), à 30 % d'une répétition maximum (1RM).
2) BFR-RE avec basse pression (BFR40), à 30% de 1RM.
3) BFR-RE avec haute pression (BFR80), à 30% de 1RM.
4) Exercice de résistance à charge lourde (HLRE), à 70 % d'une répétition maximum (1RM)
La pression BFR a été prescrite par rapport à la pression d'occlusion des membres à 40 % et 80 % pour les essais à basse et haute pression.
Les seuils de douleur à la pression (PPT) ont été évalués avant, 5 minutes et 24 heures après l'exercice des muscles en exercice et non en exercice.
Des échantillons de sang ont été prélevés aux mêmes moments pour déterminer les concentrations plasmatiques de bêta-endorphine et de 2-arachidonoylglycérol.
Tous les exercices ont été effectués avec le membre inférieur dominant. Les contractions ont été effectuées dans une plage de 0 à 90° de flexion du genou selon un cycle de contraction de 1,5s concentrique et 1,5s excentrique, évalué à l'aide d'un métronome.
Au cours des essais LLRE et BFR40 et BFR80, les participants ont effectué 4 séries (30, 15, 15 et 15 répétitions) de leg press monopodal à 30 % 1RM avec des périodes de repos de 30 s entre les séries.
Au cours des essais FBR40 et FBR80, le BFR a été appliqué en continu pendant toutes les périodes d'exercice et de repos à 40 % et 80 % de la « limb occlusion pressure » (LOP).
Au cours de l'essai HLRE, les participants ont effectué 4 x 10 répétitions de l'exercice de leg presse à 70 % de 1RM. L'évaluation de la perception de l'effort (RPE) et de la douleur des participants a été effectuée à l'aide de l’échelle de Borg.
Douze personnes ont réalisé quatre essais expérimentaux impliquant un exercice unilatéral (leg press) :
Quatre protocoles d'exercices de résistance ont été utilisés dans un ordre aléatoire, dont
1) Exercice de résistance à charge légère (LLRE), à 30 % d'une répétition maximum (1RM).
2) BFR-RE avec basse pression (BFR40), à 30% de 1RM.
3) BFR-RE avec haute pression (BFR80), à 30% de 1RM.
4) Exercice de résistance à charge lourde (HLRE), à 70 % d'une répétition maximum (1RM)
La pression BFR a été prescrite par rapport à la pression d'occlusion des membres à 40 % et 80 % pour les essais à basse et haute pression.
Les seuils de douleur à la pression (PPT) ont été évalués avant, 5 minutes et 24 heures après l'exercice des muscles en exercice et non en exercice.
Des échantillons de sang ont été prélevés aux mêmes moments pour déterminer les concentrations plasmatiques de bêta-endorphine et de 2-arachidonoylglycérol.
Tous les exercices ont été effectués avec le membre inférieur dominant. Les contractions ont été effectuées dans une plage de 0 à 90° de flexion du genou selon un cycle de contraction de 1,5s concentrique et 1,5s excentrique, évalué à l'aide d'un métronome.
Au cours des essais LLRE et BFR40 et BFR80, les participants ont effectué 4 séries (30, 15, 15 et 15 répétitions) de leg press monopodal à 30 % 1RM avec des périodes de repos de 30 s entre les séries.
Au cours des essais FBR40 et FBR80, le BFR a été appliqué en continu pendant toutes les périodes d'exercice et de repos à 40 % et 80 % de la « limb occlusion pressure » (LOP).
Au cours de l'essai HLRE, les participants ont effectué 4 x 10 répétitions de l'exercice de leg presse à 70 % de 1RM. L'évaluation de la perception de l'effort (RPE) et de la douleur des participants a été effectuée à l'aide de l’échelle de Borg.
Résultats
Paramètres de l'exercice
Les 12 participants ont terminé tous les essais expérimentaux sans aucun événement indésirable. La charge et le volume total d'exercice était plus important dans le HLRE.
La pression BFR était plus élevée dans l'essai BFR80 par rapport à BFR40.
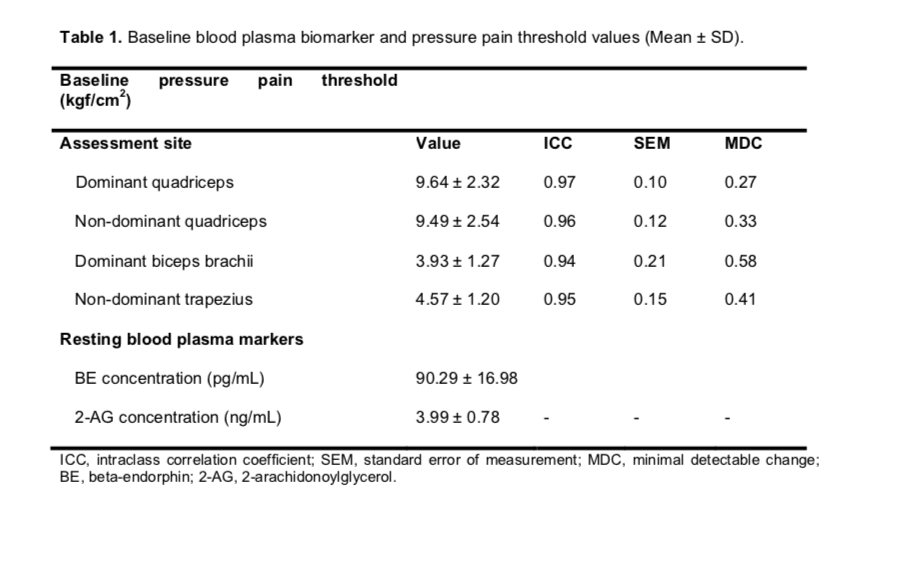
PPT de base
Aucune différence de seuil de douleur à la pression n’a été constatée entre les 4 essais expérimentaux.
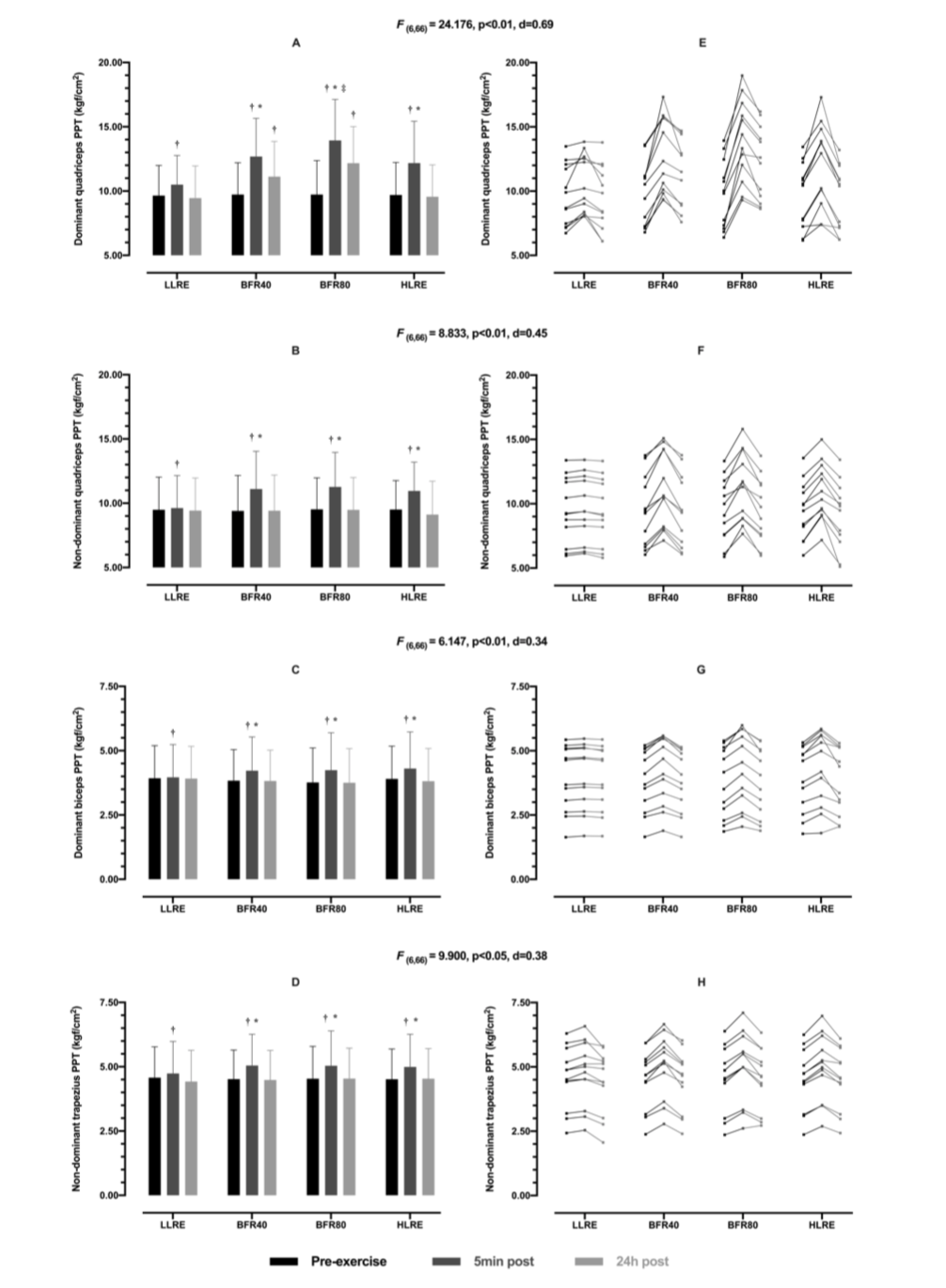
Changement de PPT avec exercice de résistance
Le BFR-RE à haute pression a augmenté les PPTs dans le membre en exercice dans une plus grande mesure que tous les autres essais.
Des effets EIH systémiques comparables ont été observés avec les essais HLRE et les deux essais BFR-RE.
Les PPTs dans le membre en exercice sont restés élevés au-dessus de la ligne de base 24 heures post exercice après les deux essais BFR-RE.
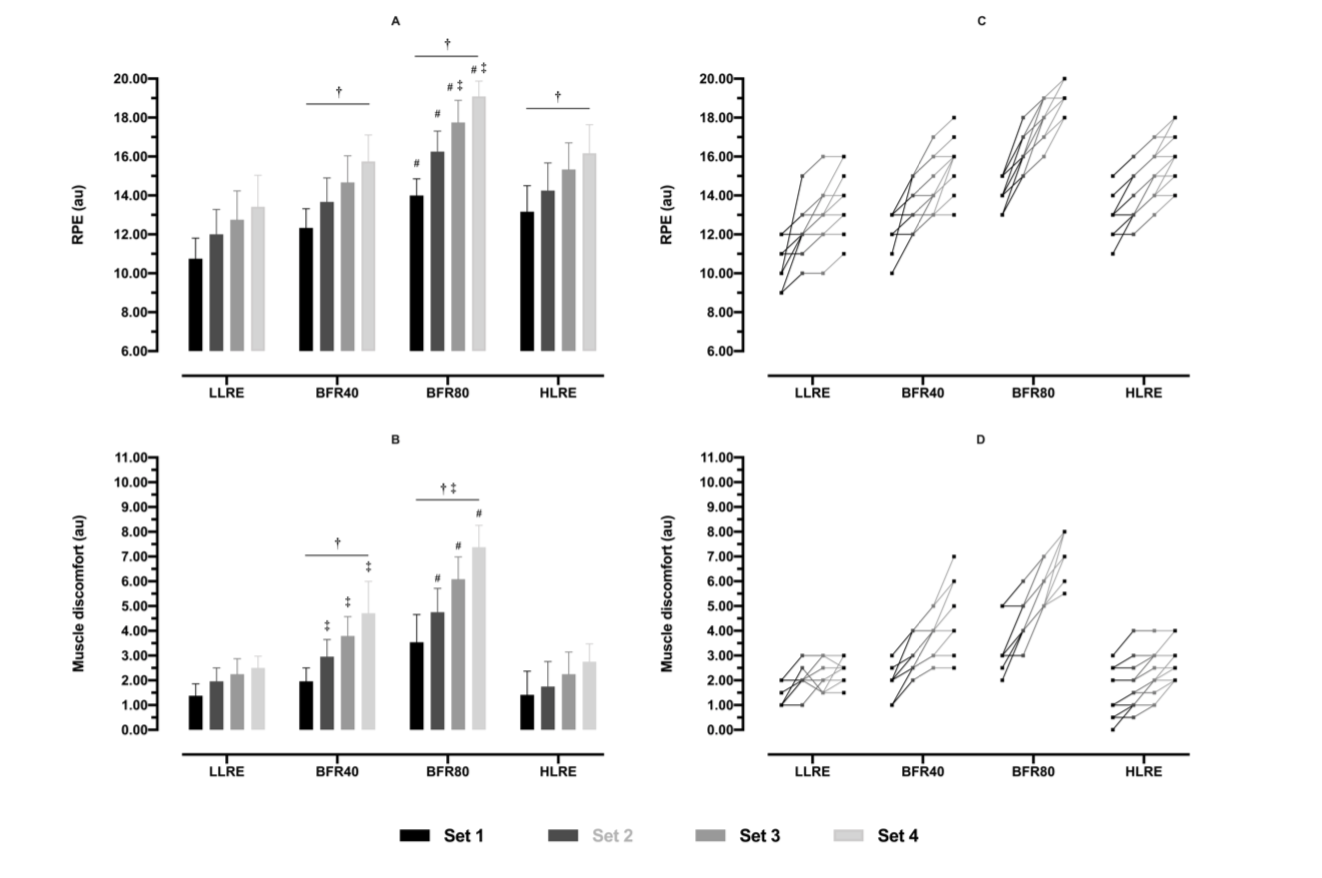
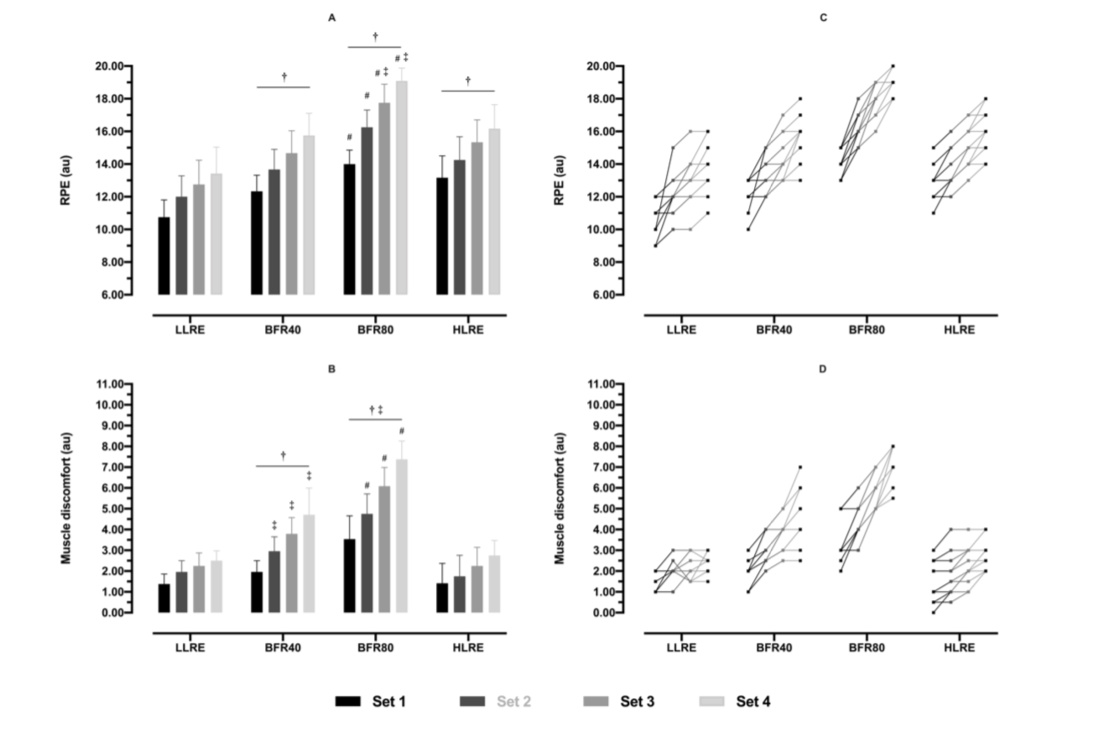
RPE
Le RPE a augmenté après chaque série d'exercices par rapport à la série précédente pour toutes les conditions.
Le RPE était plus élevée dans le cas du FBR80 que dans celui du FBR40 et de l’HLRE.
Inconfort musculaire
L'inconfort musculaire a augmenté après chaque série d'exercices par rapport à la série précédente pour toutes les conditions.
La gêne musculaire était plus importante avec BFR40 et BFR80 qu’avec les HLRE.
La gêne musculaire était plus importante avec BFR80 que BFR40.
Niveaux de plasma BE et 2AG
- Il n'y a pas eu de changement de la concentration plasmatique de bêta-endorphine après l'exercice dans tous les essais.
L'augmentation du BE a été significativement plus importante après l'exercice pour le BFR40 et le BFR80 que pour le HLRE.
Il n'y a pas eu de différences dans le BE à 24h après l'exercice par rapport au pré-exercice après LLRE, BFR40, BFR80 et HLRE.
- Aucune modification de la concentration de 2-arachidonoylglycérol n'a été observée.
Paramètres de l'exercice
Les 12 participants ont terminé tous les essais expérimentaux sans aucun événement indésirable. La charge et le volume total d'exercice était plus important dans le HLRE.
La pression BFR était plus élevée dans l'essai BFR80 par rapport à BFR40.
PPT de base
Aucune différence de seuil de douleur à la pression n’a été constatée entre les 4 essais expérimentaux.
Changement de PPT avec exercice de résistance
Le BFR-RE à haute pression a augmenté les PPTs dans le membre en exercice dans une plus grande mesure que tous les autres essais.
Des effets EIH systémiques comparables ont été observés avec les essais HLRE et les deux essais BFR-RE.
Les PPTs dans le membre en exercice sont restés élevés au-dessus de la ligne de base 24 heures post exercice après les deux essais BFR-RE.
RPE
Le RPE a augmenté après chaque série d'exercices par rapport à la série précédente pour toutes les conditions.
Le RPE était plus élevée dans le cas du FBR80 que dans celui du FBR40 et de l’HLRE.
Inconfort musculaire
L'inconfort musculaire a augmenté après chaque série d'exercices par rapport à la série précédente pour toutes les conditions.
La gêne musculaire était plus importante avec BFR40 et BFR80 qu’avec les HLRE.
La gêne musculaire était plus importante avec BFR80 que BFR40.
Niveaux de plasma BE et 2AG
- Il n'y a pas eu de changement de la concentration plasmatique de bêta-endorphine après l'exercice dans tous les essais.
L'augmentation du BE a été significativement plus importante après l'exercice pour le BFR40 et le BFR80 que pour le HLRE.
Il n'y a pas eu de différences dans le BE à 24h après l'exercice par rapport au pré-exercice après LLRE, BFR40, BFR80 et HLRE.
- Aucune modification de la concentration de 2-arachidonoylglycérol n'a été observée.

Discussion
La présente étude contient plusieurs conclusions.
Le BFR (à basse et haute pression) et le HLRE ont augmenté le seuil de douleur dans le membre en exercice par rapport au LLRE (26-48% contre 10%). Le BFR à haute pression a entraîné la plus forte augmentation PPT dans le membre en exercice (48%).
Les PPTs dans le membre en exercice sont restés élevés au-dessus de la ligne de base 24 heures post exercice après les deux essais BFR-RE.
Aucune altération de la concentration de 2-AG en circulation n'a été constatée ; cependant, la concentration de BE après l'exercice a été augmentée à basse (21%) et haute (23%) pression avec BFR-RE par rapport à LLRE (0,4%) et HLRE (5%).
Enfin, la bêta-endorphine et l'inconfort musculaire ont été considérés comme des facteurs de médiation de la relation entre l'exercice et le changement de PPT.
Dans la présente étude, il est constaté une augmentation de PPT dans les muscles qui font ou ne font pas d'exercice, dans toutes les conditions d'exercice. Les résultats de la présente étude soutiennent également l'idée que les voies nociceptives inhibitrices locales et centrales contribuent à l'hypoalgésie systémique après l'exercice.
Comme les auteurs l'ont supposé, des augmentations plus importantes des PPTs ont été observées avec HLRE (10-26%) par rapport à LLRE (1-10%). La pratique de LLRE avec BFR a entraîné des augmentations plus importantes des PPTs (11-34% et 11-48%), ce qui est conforme aux recherches précédentes qui ont démontré une plus grande réduction de la douleur pendant BFR-RE par rapport à LLRE chez les personnes souffrant de douleurs antérieures de genou. L'augmentation des PPTs dans les essais avec BFR était similaire à celle des HLRE sur tous les sites d'évaluation, sauf pour le membre en exercice où le BFR à haute pression semblait augmenter le changement (48% contre 26%). Cela peut expliquer les résultats d'études récentes dans des populations gênés par la charge, où le BFR à haute pression (60-80% LOP) réduit la douleur plus que HLRE pendant un programme d'entraînement.
La réponse d'hypoalgésie à l'exercice est généralement diminuée dans les 30 à 45 minutes qui suivent l'exercice. Une réduction de la sensibilité à la douleur à 45 minutes après le BFR-RE a été observée chez des personnes souffrant de douleurs antérieures de genou, et des preuves récentes chez des patients ayant subi une opération des ligaments du genou suggèrent que la douleur peut être réduite jusqu'à 24 heures post l'exercice.
La présente étude montre que le PPT dans le membre en exercice est restée élevée au-dessus de la ligne de base 24 heures après le BFR-RE. Cela peut expliquer les résultats précédents où les patients ont signalé une réduction de la douleur le lendemain de l’exercice BFR-RE.
Cette élévation persistante du PPT n'est probablement pas liée à la production endogène d'opioïdes, qui était revenue au niveau de référence 24 heures après l'exercice. De plus, bien qu'elle n'ait pas été mesurée, les auteurs n'ont pas anticipé la présence d'une gêne musculaire dans le membre qui fait de l'exercice le jour suivant, il est donc peu probable que l'hypoalgésie prolongée 24 heures après l'exercice soit médiée de manière CPM. La limitation de cet effet au seul membre auquel le stimulus du BFR a été appliqué suggère que l'hypoalgésie prolongée est principalement liée à l'activation de mécanismes inhibiteurs de la douleur locaux ou segmentaires, plutôt qu'à un mécanisme systémique.
Plusieurs mécanismes d'EIH ont été proposés, l'intensité de l'exercice est reconnue comme un déterminant important de l'EIH, un exercice d'intensité plus élevée entraînant une plus grande EIH.
L’étude fournit des preuves d'une plus grande EIH avec le BFR-RE par rapport au LLRE sans BFR, pour lequel plusieurs explications sont possibles.
Le stimulus du BFR peut avoir agi comme un stimulus de conditionnement nocif dans un mécanisme de modulation conditionnée de la douleur (CPM), par lequel "la douleur inhibe la douleur".
La perception de l'inconfort et de la douleur est exacerbée pendant le BFR-RE dans une mesure similaire ou supérieure à celle du HLRE. Ceci est souvent attribué à la stimulation des fibres afférentes des groupes III et IV et à une augmentation ultérieure de l'activité nerveuse sympathique et de la perception de la douleur et de l'inconfort.
L'inconfort musculaire était plus important dans le membre qui faisait de l'exercice dans les exercices avec BFR-RE, et les résultats de l'analyse de la médiation montrent que l'inconfort musculaire est le médiateur de la relation entre l'intervention de l'exercice et le changement de PPT, ce qui indique un lien entre la douleur et l'inconfort générés pendant l'exercice et la réponse de l'EIH. L'augmentation plus importante de la PPT ainsi que les scores d'inconfort plus élevés dans le membre qui fait de l'exercice avec BFR haute pression par rapport à BFR basse pression corroboreraient ce fait. Cela serait également en accord avec les recherches existantes qui montrent que le niveau de EIH est plus important après un exercice douloureux par rapport à un exercice non douloureux.
Le BFR-RE est souvent associé à une sensation d’engourdissement ; il a été suggéré que la pression appliquée sur le nerf périphérique entraîne une ischémie et un blocage de la conduction nerveuse, ce qui pourrait éventuellement modifier la sensation de douleur avec le BFR-RE. Bien que les auteurs n'aient pas mesuré la vitesse de conduction nerveuse dans la présente étude, Clark et al., n'ont constaté aucun changement de la vitesse de conduction nerveuse avant et après 4 semaines d'entraînement à la résistance au BFR-RE.
De plus, comme tout effet secondaire de la compression nerveuse est rapidement réversible, il est peu probable que l'élévation des PPT à 24 heures après le BFR-RE dans la présente étude soit due à des altérations de la fonction neurale.
Conformément à des recherches antérieures sur l'homme, l'étude actuelle a démontré une augmentation significative de la concentration de BE dans le sang périphérique suite à un exercice BFR-RE. Cela suggère l'implication d'un mécanisme à médiation opioïde dans l'EIH avec le BFR-RE.
Les résultats des analyses de médiation le confirmeraient. L'activation du système opioïde endogène et la stimulation de la production de BE peuvent contribuer à la réponse de l'EIH en inhibant l'activité nocive évoquée.
Le corps produit du BE en réponse à des facteurs de stress physiologiques tels que la douleur et l'exercice ; on pense que ce dernier est causé par la stimulation des fibres afférentes des groupes III et IV dans les muscles contractés pendant l'exercice. Un niveau élevé de stress métabolique est généré pendant le BFR-RE, indiqué par l'ischémie, l'hypoxie, l'accumulation intramusculaire de métabolites et une réduction du pH des tissus. Cela peut activer les fibres afférentes des groupes III et IV et on pense que cela entraîne une plus grande perception de l'intensité et de l'inconfort associés au BFR-RE.
En effet, dans la présente étude, les participants ont rapporté un RPE plus important avec BFR-RE qu’avec LLRE. La perception accrue de l'exercice avec le BFR-RE est souvent attribuée à la stimulation des fibres afférentes des groupes III et IV et à la rétroaction afférente.
Une perception accrue de l'inconfort dans le muscle en exercice, une perception accrue de l'effort peut avoir contribué à la stimulation de la production endogène d'opioïdes.
Les résultats de Heyman et al., confirmeraient cette notion, car les auteurs ont observé une augmentation de la concentration de BE uniquement lorsque l'intensité de l'exercice était élevée. Il est important de noter que les endorphines ne semblent pas traverser la barrière hémato-encéphalique et ne peuvent donc pas être considérées comme indicatives d'effets centraux, ce qui constitue une limitation de l'examen de BE dans la circulation systémique par rapport à l'EIH.
Contrairement à notre hypothèse, nous n'avons pas observé de changement de la concentration de 2-AG dans le sang périphérique après l'exercice dans aucune des conditions expérimentales.
Des recherches antérieures n'ont montré aucun changement de la concentration de 2-AG après un exercice intense, alors qu'un autre endocannabinoïde, connu sous le nom d'anandamide, a augmenté, ce qui peut être déterminé par leurs différentes voies métaboliques.
Les recherches sur les animaux montrent qu'en manipulant la durée et l'intensité du facteur de stress de l'exercice, il est possible de déclencher des mécanismes d'hypoalgésie opioïdes ou non opioïdes. Par conséquent, les propriétés de l'exercice lui-même peuvent être un facteur important pour déterminer l'activation des mécanismes endogènes d'inhibition de la douleur.
Malgré ces limitations, plusieurs implications importantes peuvent être tirées de la présente étude. Bien que l'EIH soit généralement plus importante avec une intensité plus élevée et un exercice prolongé, les résultats ici montrent que l'ajout du BFR à LLRE peut maximiser la réponse de l'EIH obtenue lors d'un exercice de faible intensité dans une mesure similaire ou supérieure à celle de l'HLRE.
Cela a des implications importantes pour les personnes souffrant de douleurs aiguës et chroniques ou la charge n’est pas possible.
Les résultats de cette étude fournissent également des preuves d'hypoalgésie systémique après un exercice unilatéral, ce qui suggère que l’on peut obtenir un soulagement de la douleur avec des exercices sur les membres non affectés ou sans douleur. Enfin, nos résultats suggèrent que le BFR-RE peut prolonger l'effet d'hypoalgésie dans le membre auquel le BFR est appliqué jusqu'à 24 heures.
La présente étude contient plusieurs conclusions.
Le BFR (à basse et haute pression) et le HLRE ont augmenté le seuil de douleur dans le membre en exercice par rapport au LLRE (26-48% contre 10%). Le BFR à haute pression a entraîné la plus forte augmentation PPT dans le membre en exercice (48%).
Les PPTs dans le membre en exercice sont restés élevés au-dessus de la ligne de base 24 heures post exercice après les deux essais BFR-RE.
Aucune altération de la concentration de 2-AG en circulation n'a été constatée ; cependant, la concentration de BE après l'exercice a été augmentée à basse (21%) et haute (23%) pression avec BFR-RE par rapport à LLRE (0,4%) et HLRE (5%).
Enfin, la bêta-endorphine et l'inconfort musculaire ont été considérés comme des facteurs de médiation de la relation entre l'exercice et le changement de PPT.
Dans la présente étude, il est constaté une augmentation de PPT dans les muscles qui font ou ne font pas d'exercice, dans toutes les conditions d'exercice. Les résultats de la présente étude soutiennent également l'idée que les voies nociceptives inhibitrices locales et centrales contribuent à l'hypoalgésie systémique après l'exercice.
Comme les auteurs l'ont supposé, des augmentations plus importantes des PPTs ont été observées avec HLRE (10-26%) par rapport à LLRE (1-10%). La pratique de LLRE avec BFR a entraîné des augmentations plus importantes des PPTs (11-34% et 11-48%), ce qui est conforme aux recherches précédentes qui ont démontré une plus grande réduction de la douleur pendant BFR-RE par rapport à LLRE chez les personnes souffrant de douleurs antérieures de genou. L'augmentation des PPTs dans les essais avec BFR était similaire à celle des HLRE sur tous les sites d'évaluation, sauf pour le membre en exercice où le BFR à haute pression semblait augmenter le changement (48% contre 26%). Cela peut expliquer les résultats d'études récentes dans des populations gênés par la charge, où le BFR à haute pression (60-80% LOP) réduit la douleur plus que HLRE pendant un programme d'entraînement.
La réponse d'hypoalgésie à l'exercice est généralement diminuée dans les 30 à 45 minutes qui suivent l'exercice. Une réduction de la sensibilité à la douleur à 45 minutes après le BFR-RE a été observée chez des personnes souffrant de douleurs antérieures de genou, et des preuves récentes chez des patients ayant subi une opération des ligaments du genou suggèrent que la douleur peut être réduite jusqu'à 24 heures post l'exercice.
La présente étude montre que le PPT dans le membre en exercice est restée élevée au-dessus de la ligne de base 24 heures après le BFR-RE. Cela peut expliquer les résultats précédents où les patients ont signalé une réduction de la douleur le lendemain de l’exercice BFR-RE.
Cette élévation persistante du PPT n'est probablement pas liée à la production endogène d'opioïdes, qui était revenue au niveau de référence 24 heures après l'exercice. De plus, bien qu'elle n'ait pas été mesurée, les auteurs n'ont pas anticipé la présence d'une gêne musculaire dans le membre qui fait de l'exercice le jour suivant, il est donc peu probable que l'hypoalgésie prolongée 24 heures après l'exercice soit médiée de manière CPM. La limitation de cet effet au seul membre auquel le stimulus du BFR a été appliqué suggère que l'hypoalgésie prolongée est principalement liée à l'activation de mécanismes inhibiteurs de la douleur locaux ou segmentaires, plutôt qu'à un mécanisme systémique.
Plusieurs mécanismes d'EIH ont été proposés, l'intensité de l'exercice est reconnue comme un déterminant important de l'EIH, un exercice d'intensité plus élevée entraînant une plus grande EIH.
L’étude fournit des preuves d'une plus grande EIH avec le BFR-RE par rapport au LLRE sans BFR, pour lequel plusieurs explications sont possibles.
Le stimulus du BFR peut avoir agi comme un stimulus de conditionnement nocif dans un mécanisme de modulation conditionnée de la douleur (CPM), par lequel "la douleur inhibe la douleur".
La perception de l'inconfort et de la douleur est exacerbée pendant le BFR-RE dans une mesure similaire ou supérieure à celle du HLRE. Ceci est souvent attribué à la stimulation des fibres afférentes des groupes III et IV et à une augmentation ultérieure de l'activité nerveuse sympathique et de la perception de la douleur et de l'inconfort.
L'inconfort musculaire était plus important dans le membre qui faisait de l'exercice dans les exercices avec BFR-RE, et les résultats de l'analyse de la médiation montrent que l'inconfort musculaire est le médiateur de la relation entre l'intervention de l'exercice et le changement de PPT, ce qui indique un lien entre la douleur et l'inconfort générés pendant l'exercice et la réponse de l'EIH. L'augmentation plus importante de la PPT ainsi que les scores d'inconfort plus élevés dans le membre qui fait de l'exercice avec BFR haute pression par rapport à BFR basse pression corroboreraient ce fait. Cela serait également en accord avec les recherches existantes qui montrent que le niveau de EIH est plus important après un exercice douloureux par rapport à un exercice non douloureux.
Le BFR-RE est souvent associé à une sensation d’engourdissement ; il a été suggéré que la pression appliquée sur le nerf périphérique entraîne une ischémie et un blocage de la conduction nerveuse, ce qui pourrait éventuellement modifier la sensation de douleur avec le BFR-RE. Bien que les auteurs n'aient pas mesuré la vitesse de conduction nerveuse dans la présente étude, Clark et al., n'ont constaté aucun changement de la vitesse de conduction nerveuse avant et après 4 semaines d'entraînement à la résistance au BFR-RE.
De plus, comme tout effet secondaire de la compression nerveuse est rapidement réversible, il est peu probable que l'élévation des PPT à 24 heures après le BFR-RE dans la présente étude soit due à des altérations de la fonction neurale.
Conformément à des recherches antérieures sur l'homme, l'étude actuelle a démontré une augmentation significative de la concentration de BE dans le sang périphérique suite à un exercice BFR-RE. Cela suggère l'implication d'un mécanisme à médiation opioïde dans l'EIH avec le BFR-RE.
Les résultats des analyses de médiation le confirmeraient. L'activation du système opioïde endogène et la stimulation de la production de BE peuvent contribuer à la réponse de l'EIH en inhibant l'activité nocive évoquée.
Le corps produit du BE en réponse à des facteurs de stress physiologiques tels que la douleur et l'exercice ; on pense que ce dernier est causé par la stimulation des fibres afférentes des groupes III et IV dans les muscles contractés pendant l'exercice. Un niveau élevé de stress métabolique est généré pendant le BFR-RE, indiqué par l'ischémie, l'hypoxie, l'accumulation intramusculaire de métabolites et une réduction du pH des tissus. Cela peut activer les fibres afférentes des groupes III et IV et on pense que cela entraîne une plus grande perception de l'intensité et de l'inconfort associés au BFR-RE.
En effet, dans la présente étude, les participants ont rapporté un RPE plus important avec BFR-RE qu’avec LLRE. La perception accrue de l'exercice avec le BFR-RE est souvent attribuée à la stimulation des fibres afférentes des groupes III et IV et à la rétroaction afférente.
Une perception accrue de l'inconfort dans le muscle en exercice, une perception accrue de l'effort peut avoir contribué à la stimulation de la production endogène d'opioïdes.
Les résultats de Heyman et al., confirmeraient cette notion, car les auteurs ont observé une augmentation de la concentration de BE uniquement lorsque l'intensité de l'exercice était élevée. Il est important de noter que les endorphines ne semblent pas traverser la barrière hémato-encéphalique et ne peuvent donc pas être considérées comme indicatives d'effets centraux, ce qui constitue une limitation de l'examen de BE dans la circulation systémique par rapport à l'EIH.
Contrairement à notre hypothèse, nous n'avons pas observé de changement de la concentration de 2-AG dans le sang périphérique après l'exercice dans aucune des conditions expérimentales.
Des recherches antérieures n'ont montré aucun changement de la concentration de 2-AG après un exercice intense, alors qu'un autre endocannabinoïde, connu sous le nom d'anandamide, a augmenté, ce qui peut être déterminé par leurs différentes voies métaboliques.
Les recherches sur les animaux montrent qu'en manipulant la durée et l'intensité du facteur de stress de l'exercice, il est possible de déclencher des mécanismes d'hypoalgésie opioïdes ou non opioïdes. Par conséquent, les propriétés de l'exercice lui-même peuvent être un facteur important pour déterminer l'activation des mécanismes endogènes d'inhibition de la douleur.
Malgré ces limitations, plusieurs implications importantes peuvent être tirées de la présente étude. Bien que l'EIH soit généralement plus importante avec une intensité plus élevée et un exercice prolongé, les résultats ici montrent que l'ajout du BFR à LLRE peut maximiser la réponse de l'EIH obtenue lors d'un exercice de faible intensité dans une mesure similaire ou supérieure à celle de l'HLRE.
Cela a des implications importantes pour les personnes souffrant de douleurs aiguës et chroniques ou la charge n’est pas possible.
Les résultats de cette étude fournissent également des preuves d'hypoalgésie systémique après un exercice unilatéral, ce qui suggère que l’on peut obtenir un soulagement de la douleur avec des exercices sur les membres non affectés ou sans douleur. Enfin, nos résultats suggèrent que le BFR-RE peut prolonger l'effet d'hypoalgésie dans le membre auquel le BFR est appliqué jusqu'à 24 heures.
Conclusion
- Le BFR-RE à haute pression a provoqué la plus grande réponse EIH dans le membre en exercice et un effet systémique a été observé dans une moindre mesure, qui était comparable au HLRE avec BFR-RE.
- Le BFR-RE à basse et haute pression a prolongé l'effet d'hypoalgésie jusqu'à 24 heures dans le membre auquel le BFR a été appliqué.
- Les mécanismes qui sous-tendent l'EIH avec le BFR-RE peuvent être liés au système opioïde et à un effet de modulation de la douleur conditionnée plutôt qu'à des mécanismes à médiation endocannabinoïde et associés au stress physiologique accru du BFR-RE.
- Pour la première fois, cette étude fournit des preuves des mécanismes et de l'effet hypoalgésique du BFR-RE et souligne son utilité possible dans les exercices pour les populations souffrant de douleurs aiguës, chroniques et dont la charge n’est pas possible.
Article de référence
Hughes L, Patterson SD. The effect of blood flow restriction exercise on exercise-induced hypoalgesia and endogenous opioid and endocannabinoid mechanisms of pain modulation. J Appl Physiol (1985). 2020 Feb 27.
Hughes L, Patterson SD. The effect of blood flow restriction exercise on exercise-induced hypoalgesia and endogenous opioid and endocannabinoid mechanisms of pain modulation. J Appl Physiol (1985). 2020 Feb 27.




 L'effet induit par l’exercice de restriction de flux sanguin sur l'hypoalgésie et les mécanismes endogènes opioïdes et endocannabinoïdes de modulation de la douleur
L'effet induit par l’exercice de restriction de flux sanguin sur l'hypoalgésie et les mécanismes endogènes opioïdes et endocannabinoïdes de modulation de la douleur